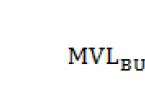Периодический закон открыт в 18. Открытие периодического закона химических элементов Д.И
Здесь читатель найдет информацию об одном из важнейших законов, когда-либо открытых человеком в научной области - периодическом законе Менделеева Дмитрия Ивановича. Вы ознакомитесь с его значением и влиянием на химию, будут рассмотрены общие положения, характеристика и детали периодического закона, история открытия и основные положения.
Что такое периодический закон
Периодический закон - это природный закон фундаментального характера, который был открыт впервые Д. И. Менделеевым еще в 1869 году, а само открытие произошло благодаря сравнению свойств некоторых химических элементов и величин массы атома, известных в те времена.
Менделеев утверждал, что, согласно его закону, простые и сложные тела и разнообразные соединения элементов зависят от их зависимости периодического типа и от веса их атома.
Периодический закон является уникальным в своем роде и это связано с тем фактом, что он не выражается математическими уравнениями в отличие от других фундаментальных законов природы и вселенной. Графически свое выражение он находит в периодической системе химических элементов.
История открытия
Открытие периодического закона произошло в 1869 году, но попытки систематизировать все известные х-кие элементы начались задолго до этого.
Первую попытку создать такую систему предпринял И. В. Деберейнер в 1829. Он классифицировал все известные ему химические элементы в триады, связанные между собой близостью половины суммы атомных масс, входящих в эту группу трех компонентов. Следом за Деберейнером предприняли попытку создать уникальную таблицу классификации элементов А. де Шанкуртуа, он назвал свою систему «земной спиралью», а после него была составлена Джоном Ньюлендсом октава Ньюлендса. В 1864 практически одновременно Уильям Олдинг и Лотар Мейер опубликовали созданные независимо друг от друга таблицы.

Периодический закон был представлен научному сообществу на обозрение восьмого марта 1869, и произошло это во время заседания Русского х-кого общества. Менделеев Дмитрий Иванович заявил при всех о своем открытии и в том же году был выпущен менделеевский учебник «Основы химии», где впервые была показана периодическая таблица, созданная им. Годом позже, в 1870, он написал статью и отдал ее на обозрение в РХО, где впервые было употреблено понятие периодического закона. В 1871 Менделеев дал исчерпывающую характеристику своего з-на в знаменитой статье периодической законности химических элементов.

Неоценимый вклад в развитие химии
Значение периодического закона невероятно велико для научного сообщества всего мира. Это связано с тем, что открытие его дало мощный толчок развитию, как химии, так и других наук о природе, например, физике и биологии. Открытой была взаимосвязь элементов с их качественными химическими и физическими характеристиками, также это позволило понять суть построения всех элементов по одному принципу и дало начало современной формулировке понятий о химических элементах, конкретизировать знания представление о веществах сложного и простого строения.
Использование периодического закона позволило решать проблему химического прогнозирования, определить причину поведения известных химических элементов. Атомная физика, а в том числе и ядерная энергетика, стали возможными вследствие этого же закона. В свою очередь, данные науки позволили расширить горизонты сущности этого закона и углубиться в его понимание.
Химические свойства элементов периодической системы
По сути, химические элементы взаимосвязаны между собой характеристиками, свойственными им в состоянии свободного как атома, так и иона, сольватированного или гидратированного, в простом веществе и форме, которую могут образовать их многочисленные соединения. Однако х-кие свойства обычно заключаются в двух явлениях: свойства, характерные для атома в свободном состоянии, и простого вещества. К такому роду свойств относится множество их видов, но самые важные это:
- Атомная ионизация и ее энергия, зависящая от положения элемента в таблице, его порядкового числа.
- Энергетическое родство атома и электрона, которая так же, как и атомная ионизация, зависит от места нахождения элемента в периодической таблице.
- Электроотрицательность атома, не носящая постоянное значение, а способная изменяться в зависимости от различного рода факторов.
- Радиусы атомов и ионов - тут, как правило, используются эмпирические данные, что связано с волновой природой электронов в состоянии движения.
- Атомизация простых веществ - описание возможностей элемента к реакционной способности.
- Степени окисления - формальная характеристика, однако фигурирующая как одна из важнейших характеристик элемента.
- Потенциал окисления для простых веществ - это измерение и показание потенциала вещества к действию его в водных растворах, а также уровень проявления свойств окислительно-восстановительного характера.

Периодичность элементов внутреннего и вторичного типа
Периодический закон дает понимание еще одной немаловажной составной частицы природы - внутренней и вторичной периодичности. Вышеупомянутые области изучения атомных свойств, на самом деле, гораздо сложнее, чем можно подумать. Связано это с тем фактом, что элементы s, p, d таблицы меняют свои качественные характеристики в зависимости от положения в периоде (периодичность внутреннего характера) и группе (периодичность вторичного характера). Например, внутренний процесс перехода элемента s от первой группы до восьмой к p-элементу сопровождается точками минимума и максимума на кривой линии энергии ионизированного атома. Данное явление показывает внутреннюю непостоянность периодичности изменения свойств атома по положению в периоде.

Итоги
Теперь читатель имеет четкое понимание и определение того, что являет собой периодический закон Менделеева, осознает его значение для человека и развития различных наук и имеет представление о его современных положениях и истории открытия.
ЗАНЯТИЕ 5 10-й класс (первый год обучения)
Периодический закон и система химических элементов д.И.Менделеева План
1. История открытия периодического закона и системы химических элементов Д.И.Менделеева.
2. Периодический закон в формулировке Д.И.Менделеева.
3. Современная формулировка периодического закона.
4. Значение периодического закона и системы химических элементов Д.И.Менделеева.
5. Периодическая система химических элементов – графическое отражение периодического закона. Строение периодической системы: периоды, группы, подгруппы.
6. Зависимость свойств химических элементов от строения их атомов.
1 марта (по новому стилю) 1869 г. считается датой открытия одного из важнейших законов химии – периодического закона. В середине XIX в. было известно 63 химических элемента, и возникла потребность в их классификации. Попытки такой классификации предпринимали многие ученые (У.Одлинг и Дж.А.Р.Ньюлендс, Ж.Б.А.Дюма и А.Э.Шанкуртуа, И.В.Деберейнер и Л.Ю.Мейер), но лишь Д.И.Менделееву удалось увидеть определенную закономерность, расположив элементы в порядке возрастания их атомных масс. Эта закономерность имеет периодический характер, поэтому Менделеев сформулировал открытый им закон следующим образом: свойства элементов, а также формы и свойства их соединений находятся в периодической зависимости от величины атомной массы элемента.
В системе химических элементов, предложенной Менделеевым, был ряд противоречий, которые сам автор периодического закона устранить не смог (аргон–калий, теллур–йод, кобальт–никель). Лишь в начале XX в., после открытия строения атома, был объяснен физический смысл периодического закона и появилась его современная формулировка: свойства элементов, а также формы и свойства их соединений находятся в периодической зависимости от величины заряда ядер их атомов.Такую формулировку подтверждает и наличие изотопов, химические свойства которых одинаковы, хотя атомные массы различны.
Периодический закон – один из основных законов природы и важнейший закон химии. С открытия этого закона начинается современный этап развития химической науки. Хотя физический смысл периодического закона стал понятен только после создания теории строения атома, сама эта теория развивалась на основе периодического закона и системы химических элементов. Закон помогает ученым создавать новые химические элементы и новые соединения элементов, получать вещества с нужными свойствами. Сам Менделеев предсказал существование 12 элементов, которые в то время еще не были открыты, и определил их положение в периодической системе. Свойства трех из этих элементов он подробно описал, и при жизни ученого эти элементы были открыты («экабор» – галлий, «экаалюминий» – скандий, «экасилиций» – германий). Кроме того, периодический закон имеет большое философское значение, подтверждая наиболее общие законы развития природы.
Графическим отражением периодического закона является периодическая система химических элементов Менделеева. Существует несколько форм периодической системы (короткая, длинная, лестничная (предложена Н.Бором), спиралеобразная). В России наибольшее распространение получила короткая форма. Современная периодическая система содержит 110 открытых на сегодняшний день химических элементов, каждый из которых занимает определенное место, имеет свой порядковый номер и название. В таблице выделяют горизонтальные ряды – периоды (1–3 – малые, состоят из одного ряда; 4–6 – большие, состоят из двух рядов; 7-й период – незавершенный). Кроме периодов выделяют вертикальные ряды – группы, каждая из которых подразделяется на две подгруппы (главную – а и побочную – б). Побочные подгруппы содержат элементы только больших периодов, все они проявляют металлические свойства. Элементы одной подгруппы имеют одинаковое строение внешних электронных оболочек, что обусловливает их схожие химические свойства.
Период – это последовательность элементов (от щелочного металла до инертного газа), атомы которых имеют одинаковое число энергетических уровней, равное номеру периода.
Главная подгруппа – это вертикальный ряд элементов, атомы которых имеют одинаковое число электронов на внешнем энергетическом уровне. Это число равно номеру группы (кроме водорода и гелия).
Все элементы в периодической системе разделяются на 4 электронных семейства (s -, p -, d -, f -элементы) в зависимости от того, какой подуровень в атоме элемента заполняется последним.
Побочная подгруппа – это вертикальный ряд d -элементов, имеющих одинаковое суммарное число электронов на d -подуровне предвнешнего слоя и s -подуровне внешнего слоя. Это число обычно равно номеру группы.
Важнейшими свойствами химических элементов являются металличность и неметалличность.
Металличность – это способность атомов химического элемента отдавать электроны. Количественной характеристикой металличности является энергия ионизации.
Энергия ионизации атома – это количество энергии, которое необходимо для отрыва электрона от атома элемента, т. е. для превращения атома в катион. Чем меньше энергия ионизации, тем легче атом отдает электрон, тем сильнее металлические свойства элемента.
Неметалличность – это способность атомов химического элемента присоединять электроны. Количественной характеристикой неметалличности является сродство к электрону.
Сродство к электрону – это энергия, которая выделяется при присоединении электрона к нейтральному атому, т. е. при превращении атома в анион. Чем больше сродство к электрону, тем легче атом присоединяет электрон, тем сильнее неметаллические свойства элемента.
Универсальной характеристикой металличности и неметалличности является электроотрицательность (ЭО) элемента.
ЭО элемента характеризует способность его атомов притягивать к себе электроны, которые участвуют в образовании химических связей с другими атомами в молекуле.
Чем больше металличность, тем меньше ЭО.
Чем больше неметалличность, тем больше ЭО.
При определении значений относительной ЭО по шкале Полинга за единицу принята ЭО атома лития (ЭО(Li) = 1); самым электроотрицательным элементом является фтор (ЭО(F) = 4).
В малых периодах от щелочного металла к инертному газу:
Заряд ядер атомов увеличивается;
Число энергетических уровней не изменяется;
Число электронов на внешнем уровне увеличивается от 1 до 8;
Радиус атомов уменьшается;
Прочность связи электронов внешнего слоя с ядром увеличивается;
Энергия ионизации увеличивается;
Сродство к электрону увеличивается;
ЭО увеличивается;
Металличность элементов уменьшается;
Неметалличность элементов увеличивается.
Все d -элементы данного периода похожи по своим свойствам – все они являются металлами, имеют мало различающиеся радиусы атомов и значения ЭО, поскольку содержат одинаковое число электронов на внешнем уровне (например, в 4-м периоде – кроме Cr и Cu).
В главных подгруппах сверху вниз:
Число энергетических уровней в атоме увеличивается;
Число электронов на внешнем уровне одинаково;
Радиус атомов увеличивается;
Прочность связи электронов внешнего уровня с ядром уменьшается;
Энергия ионизации уменьшается;
Сродство к электрону уменьшается;
ЭО уменьшается;
Металличность элементов увеличивается;
Неметалличность элементов уменьшается.
Периодический закон Д. И. Менделеева: Свойства простых тел, а также формы и свойства соеди нений элементов находятся в периодической зависимости от величины атомных весов элементов.(Свойства эл-тов находяхтся в периодической зависимости от заряда атомов их ядер).
Периодическая система элементов. Ряды элементов, в пределах которых свойства изменяются последовательно, как, например, ряд из восьми элементов от лития до неона или от натрия до аргона, Менделеев назвал периодами. Если напишем эти два периода один под другим так, чтобы под литием находился натрий, а под неоном - аргон, то получим следующее расположение элементов:
При таком расположении в вертикальные столбцы попадают элементы, сходные по своим свойствам и обладающие одинаковой валентностью, например, литий и натрий, бериллий и магний и т. д.
Разделив все элементы на периоды и располагая один период под другим так, чтобы Сходные по свойствам и типу образуемых соединений элементы приходились друг под другом, Менделеев составил таблицу, названную им периодической системой элементов по группам и рядам.
Значение периодической систе мы. Периодическая система элементов оказала большое влияние на последующее развитие химии. Она не только была первой естественнойклассификацией химических элементов, показавшей, что они образуют стройную систему и находятся в тесной связи друг с другом, но и явилась могучим орудием для дальнейших исследований.
7. Периодическое изменение свойств химических элементов. Атомные и ионные радиусы. Энергия ионизации. Сродство к электрону. Электроотрицательность.
Зависимость атомных радиусов от заряда ядра атома Z имеет периодический характер. В пределах одного периода с увеличением Z проявляется тенденция к уменьшению размеров атома, что особенно четко наблюдается в коротких периодах
С началом застройки нового электронного слоя, более удаленного от ядра, т. е. при переходе к следующему периоду, атомные радиусы возрастают (сравните, например, радиусы атомов фтора и натрия). В результате в пределах подгруппы с возрастанием заряда ядра размеры атомов увеличиваются.
Потеря атомов электронов приводит к уменьшению его эффективных размеров, а присоединение избыточных электронов - к увеличению. Поэтому радиус положительно заряженного иона (катиона) всегда меньше, а радиус отрицательно заряженного нона (аниона) всегда больше радиуса соответствующего электронейтрального атома.
В пределах одной подгруппы радиусы ионов одинакового заряда возрастают с увеличением заряда ядра Такая закономерность объясняется увеличением числа электронных слоев и растущим удалением внешних электронов от ядра.
Наиболее характерным химическим свойством металлов является способность их атомов легко отдавать внешние электроны и превращаться в положительно заряженные ионы, а неметаллы, наоборот, характеризуются способностью присоединять электроны с образованием отрицательных ионов. Для отрыва электрона от атома с превращением последнего в положительный ион нужно затратить некоторую энергию, называемую энергией ионизации.
Энергию ионизации можно определить путем бомбардировки атомов электронами, ускоренными в электрическом поле. То наименьшее напряжение поля, при котором скорость электронов становится достаточной для ионизации атомов, называется потенциалом ионизации атомов данного элемента и выражается в вольтах. При затрате достаточной энергии можно оторвать от атома два, три и более электронов. Поэтому говорят о первом потенциале ионизации (энергия отрыва от атома первого электрона).втором потенциале ионизации (энергия отрыва второго электрона)
Как отмечалось выше, атомы могут не только отдавать, но и присоединять электроны. Энергия, выделяющаяся при присоединении электрона к свободному атому, называется сродством атома к электрону. Сродство к электрону, как и энергия ионизации, обычно выражается в электронвольтах. Так, сродство к электрону атома водорода равно 0,75 эВ, кислорода-1,47 эВ, фтора -3,52 эВ.
Сродство к электрону атомов металлов, как правило, близко к нулю или отрицательно; из этого следует, что для атомов большинства металлов присоединение электронов энергетически невыгодно. Сродство же к электрону атомов неметаллов всегда положительно и тем больше, чем ближе к благородному газу расположен неметалл в периодической системе; это свидетельствует об усилении неметаллических свойств по мере приближения к концу периода.
| " |
Махов Б.Ф.
В связи с разработкой автором «Колебательной модели нейтрального атома» с включением «мирового эфира», в которой понятия «постоянный положительный заряд атомного ядра» и «кулоновское поле» становятся излишними, встает вопрос о новой формулировке Периодического закона. Такая формулировка предлагается в данной статье, где рассматривается также проблема математического выражения Периодического закона. В статье автор использует собственный вариант «Симметричной квантовой Периодической системы нейтральных атомов (СК-ПСА)», адекватный Колебательной модели.
Всё более удаляется от нас 1869 год - время первой формулировки Периодического закона Д.И. Менделеева (ПЗМ) и разработки им Периодической системы элементов (ПСЭ-М), в которых за главный критерий упорядочения был принят атомный вес элемента, доступная тогда и более или менее понятная характеристика. Но даже сам Дмитрий Иванович говорил, что «причины периодичности мы не знаем». Тогда было известно всего 63 элемента, а об их свойствах (в основном химических) было известно мало и не всегда точно.
Тем не менее, проблема систематизации элементов уже заявила о себе и требовала решения. Гениальная интуиция Менделеева позволила ему успешно (на тогдашнем уровне знаний) справиться с задачей. Его формулировка ПЗМ (октябрь 1971): «...свойства элементов, а потому и свойства образуемых ими простых и сложных тел, стоят в периодической зависимости от их атомного веса».
Дмитрий Иванович выстроил все элементы в ряд (ряд Менделеева) по возрастанию атомного веса, в котором однако им же были допущены отступления для известных пар элементов (на основе химических свойств), т.е. фактически имеется зависимость не только от атомного веса.
Ученым стало понятно, что при переходе от одного элемента в ПСЭ-М к следующему какая-то характеристика элемента ступенчато возрастает на одну и ту же величину. Эта величина - Z получила название порядковый номер (в основном у химиков) или атомный номер (у физиков). Выяснилось, что и сам атомный вес определенным образом зависит от Z . Поэтому в качестве главного критерия упорядочения был принят порядковый номер Z, который соответственно вошел во 2-ю формулировку ПЗМ вместо атомного веса.
Шло время, и появились новые возможности систематизации. Это прежде всего успехи в исследовании линейчатых оптических спектров (ЛОС) нейтральных атомов и характеристического рентгеновского излучения (ХРИ). Выяснилось, что каждый элемент обладает уникальным спектром и целый ряд новых элементов были по ним и открыты. Для описания спектров были предложены квантовые числа, спектральные термы, принцип запрета В.Паули, закон Г.Мозли и др. Исследование атомов увенчалось созданием первых моделей атома (МОА), уже после смерти Д.И.Менделеева.
Закон Мозли, связавшего частоту характеристического рентгеновского излучения с порядковым номером Z , внес особенно большой вклад в науку. Он подтвердил правильность Менделеевского ряда и позволил указать на номера оставшихся еще неоткрытыми элементов. Но затем, руководствуясь благими намерениями придать порядковому номеру Z физический смысл, физики на уровне знаний начала XIX века (первые модели атома) пришли к поспешному выводу, что он не может быть ничем иным как постоянным положительным электрическим зарядом атомного ядра (количеством элементарных электрических зарядов - eZ).
В итоге ученые пришли к выводу, что нужна уточненная 2-я формулировка ПЗМ, в которой в качестве главного критерия систематизации был принят постоянный положительный электрический заряд ядра атома элемента.
Но, к сожалению, в начале ХХ века первые модели атома были представлены чересчур механистически (планетарные ядерные модели), а электрическая нейтральность атома в целом - положительным зарядом ядра и соответствующим количеством отрицательных элементарных частиц - электронов, т.е. тоже на уровне примитивных знаний того времени об электричестве. В результате использовались представления о постоянном кулоновском электрическом поле, притягивающем вращающиеся вокруг ядра электроны и пр. И не дай бог электрону упасть на ядро!
Открытие волновой природы электрона и многие проблемы с принятой моделью атома обусловили переход к «квантовомеханической модели атома». Квантовую механику (КВМ) объявили величайшим достижением ХХ века. Но с течением времени восторги поутихли. Причина - шаткая основа, на которой построена КВМ, базирующаяся на уравнении Шредингера, которое «описывает движение электрона». Прежде всего, неверен сам подход - вместо того, чтобы рассматривать равновесное квантовое состояние нейтрального атома в целом (на макроуровне, говоря языком синергетики), в КВМ рассматривают движение электрона (т.е. работают на излишне детализированном микроуровне). Представьте себе, что для случая идеального газа вместо рассмотрения его на макроуровне с постоянными по времени параметрами состояния газа (давлением, температурой, объемом) вдруг стали бы писать уравнения движения для каждого из миллиардов атомов и молекул газа, громко стеная при этом о трудности задачи и недостаточной мощности современных ЭВМ. В то время как на макроуровне все картина легко и изящно описывается с помощью уравнения связи параметров состояния газа - уравнения Клапейрона-Менделеева. [ФЭС, М, СЭ, 1984, с.288]
Нечто похожее по сложности предлагает нам КВМ в лице ее отцов-основателей, особенно для случая атомов с большими порядковыми номерами. Однако академик Лев Ландау (1908-68), сам один из столпов КВМ, уже писал : «Атом с более чем одним электроном представляет собой сложную систему взаимодействующих друг с другом электронов. Для такой системы можно, строго говоря, рассматривать только состояния системы в целом». Эта же идея имеется в работах физика-спектроскописта акад. АН БССР Ельяшевича М.А. (1908-95).
Однако вернемся к рассмотрению формулировок Периодического закона. Современная (уточненная 2-я) формулировка ПЗМ звучит так:
«Свойства элементов находятся в периодической зависимости от заряда их атомных ядер». Заряд ядра eZ = атомному (порядковому) номеру элемента в системе, помноженному на элементарный электрический заряд (т.е. Z численно равен количеству элементарных электрических зарядов).
Почему же нужна новая, 3-я формулировка ПЗМ?
1) Из 2-й формулировки не очень понятно, о каких свойствах идет речь - если о химических, то они не имеют прямого отношения к элементам (нейтральным атомам). При взаимодействии нейтральных атомов происходит перекрытие их переменных ЭМП, в результате они оказывают друг на друга определенную степень возбуждения. Для описания химической связи нужно знать дополнительно - что с чем соединяется (состав и структура вещества) и при каких конкретных физических условиях (КФУ) и т.д.
2) Согласно разработанной автором «Колебательной модели», у ядра нейтрального атома нет ни постоянного электрического заряда, ни создаваемого им постоянного кулоновского поля (вместо этого - пульсирующее ядро, переменное электромагнитное поле - ЭМП, стоячая ЭМВ, параметрический резонанс, высокая добротность колебаний, долговечность атома). См ФИ, 2008, № 3, с.25
3) То есть нет четкого определения ни аргумента, ни функции. Насчет характера периодической зависимости тоже нет определенности. ПЗМ бесполезен без одновременного рассмотрения самой таблицы Периодической системы, поэтому его часто вообще не упоминают в учебниках в существующей формулировке («порочный круг»). Не случайно мы до сих пор не имеем полной теории Периодической системы и самого математического выражения ПЗМ.
4) Сейчас можно использовать принципиально новые возможности для более корректной формулировки Периодического закона и вывода его математического выражения, которые дают «Колебательная модель нейтрального атома» (связанных колебаний ядра и окружающей его среды) и «Симметричная квантовая Периодическая система нейтральных атомов (СК-ПСА)», разработанные и опубликованные автором.
5) Согласно синергетическому подходу, равновесное квантовое состояние атома в целом» (макроскопический подход) может быть описано несколькими независимыми от времени параметрами. Автором показано, что ими является присущий каждому атому строго индивидуальный (принцип запрета В.Паули) набор 4-х квантовых чисел, определяемых из его ЛОС (а не из уравнений КВМ).
Такой набор квантовых чисел однозначно определяет место элемента (его координаты) в разработанной автором СК-ПСА.
6) Такие параметры должны отвечать ряду требований:
Отвечать физической природе нейтрального атома (согласно «Колебательной модели»)
Быть однозначными
Быть целочисленными (что вытекает из самой сути излучения ядра)
Легко измеряться (из спектров нейтрального атома).
Таким образом, смысл известных для каждого атома квантовых чисел должен быть уточнен согласно их физической природе.
7) Вместо уравнения КВМ Э. Шредингера автор предлагает использовать уравнения связи квантовых чисел (уравнения Махова) (автором найдены два таких уравнения) , которые и являются математическим выражением ПЗМ, адекватным новой формулировке. Подробнее об этом в готовящейся к изданию книге .
8) В свете «Колебательной модели нейтрального атома» и нового представления о переменном ЭМП ядра для новой формулировки Периодического закона вместо элементарного электрического заряда нужна другая физическая величина, вместе с порядковым номером Z характеризующая напряженность электромагнитного взаимодействия (ступенчато изменяющаяся с ростом Z) и однозначно определяемая из спектра нейтральных атомов. И такая величина есть - это постоянная тонкой структуры (α) [ФЭС-763], которую обычно используют при поисках "верхней границы Периодической системы".
Новая формулировка ПЗМ выглядит так:
«Характеристики нейтральных атомов находятся в периодической зависимости от величины напряженности (αZ ) переменного электромагнитного поля (ЭМП), создаваемого их ядрами». К такой краткой формулировке автор пришел 22 ноября 2006 г. после ряда «пространных».
Из нее видно, что вместо величины электрического заряда (eZ ), в которую входит элементарный электрический заряд, используется величина напряженности (αZ ), в которую входит α - постоянная тонкой структуры, которая «в квантовой электродинамике рассматривается как естественный параметр, характеризующий «силу» электромагнитного взаимодействия» [ФЭС, с.763].
Про характеристики нейтральных атомов (о квантовых числах, их физической природе и др.) мы уже говорили, а вот о характере периодической зависимости еще нужно немного пояснить. Уже сейчас имеются предпосылки для вывода уравнений связи квантовых чисел - это (n + l )- правила академика В.М. Клечковского (1900-72) и (n - l )- правило дхн, проф. Д.Н. Трифонова , которые использованы автором для построения СК-ПСА. Помня о переменном ЭМП и распространяющейся (на конкретную для каждого атома глубину) стоячей ЭМВ, можно сказать, что сумма этих квантовых чисел представляет полную энергию стоячей ЭМВ, а разность - глубину изменения параметра колебаний. То есть уже имеются связки квантовых чисел, которые представляют в СК-ПСА (n + l )- период (все они парные и образуют диады), а (n - l )- группы последовательных атомов - горизонтальные ряды СК-ПСА (до 4-х в периоде в пределах Z ≤ 120), представляющие собой последовательности f -, d -, p -, s - элементов. Т.е., при одном квантовом энергетическом уровне могут быть несколько квантовых состояний. Дальнейший учет особенностей двуединой стоячей ЭМВ и позволяет вывести уравнения связи квантовых чисел (уравнения Махова).
Пример: Полная энергия стоячей ЭМВ E n + l = E n + E l = const , где E n и E l - средние значения энергии электрической и магнитной составляющих ее частей.
Для прояснения физического смысла квантовых чисел воспользуемся формулой энергии квантового излучателя (в общем виде) E = Eo (2k + 1), отсюда → = 2k
Конкретно имеем для E n + l = E o (2 + 1) → = n + l , то есть сумма квантовых чисел (n + l ) - это отношение приращение полной энергии стоячей ЭМВ к ее исходному значению, что придает физический смысл упомянутому выше первому правилу академика В.М. Клечковского.
Стоячая ЭМВ - это материальный носитель параметрического резонанса (при постоянной внутренней энергии происходит перекачка энергии из электрической в магнитную и обратно с огромной частотой). При этом разность средних значений энергии электрической и магнитной составляющих полной энергии ЭМВ E n - l = E n - E l - величина изменения параметра также квантуется.
E n - l = E о (2 + 1) → = n - l , это отношение придает физический смысл правилу Д.Н Трифонова и отсюда же становится понятным правило n - l ≥ 1, так как иначе нет стоячей ЭМВ (не должно быть присущего бегущей волне n = l , и связанного с ней уноса энергии). Можно ввести понятие «относительная величина изменения параметра» : = = λ
Квантуются также средние значения составляющих полной энергии стоячей ЭМВ
E n = Eo (2n + 1) → = 2n
E l = Eo (2l + 1) → = 2l
отсюда квантовые числа n и l приобретают новый физический смысл как квантовые числа составляющих электрической и магнитной энергий полной энергии стоячей ЭМВ (вместо "главное квантовое число" и "орбитальное квантовое число").
Высокая и постоянная частота стоячей ЭМВ находит свое выражение через периодические функции, применительно к нашему случаю - тригонометрические. Двуединость стоячей ЭМВ - в параметрическом задании функции. Стоячая ЭМВ как гармоническая волна может быть описана уравнениями синусоиды вида y = A sin (ω t + φ ),
тогда n t = n cos α и l t = l sin α (параметрическое задание эллипса).
здесь n и l - квантовые числа (безразмерные целочисленные величины), показатели максимальной амплитуды относительной энергии электрической и магнитной составляющих стоячей ЭМВ, а n t и l t - текущие значения колеблющихся величин (составляющих стоячей ЭМВ) в данный момент времени , т.е. тоже величины безразмерные.*)
0 ≤ |n t | ≤ n 0 ≤ |l t | ≤ l
Поясним, что имеются именно две зависимости - косинусоида и синусоида На границе раздела «Ядро-окружающая среда» в начальный момент излучения первая имеет максимальную амплитуду - n to = n (иначе нет излучения), а амплитуда другой - l to = 0 (т.е имеется сдвиг по фазе). Начав распространяться от ядра, одна составляющая стоячей ЭМВ порождает другую и наоборот. Автор хотел бы предостеречь от поспешного вывода, что раз l to = 0, то и магнитная составляющая полной энергии стоячей ЭМВ также равна нулю. Это не так, достаточно вспомнить формулу квантового гармонического излучателя.
Вот это уравнение эллипса + = 1 (в канонической форме, обычное для связи гармонических колебаний) и представляет собой одно из уравнений связи квантовых чисел.
Физический смысл данного уравнения связи становится более ясным, если произвести некоторые преобразования. Для этого воспользуемся представлением эллипса как гипотрохоиды .
![]()
Для нашего случая ; .

Это - 1-е уравнение связи квантовых чисел (уравнение Махова).
Или достаточно наглядно ![]() .
.
Видно, что уравнение отражает постоянство полной энергии стоячей ЭМВ. Таким образом, вышеупомянутые связки квантовых чисел (n + l )- номер периода в СК-ПСА, а (n - l )- определяет последовательность местоположения входящих в состав периода горизонтальных рядов - нашли своё место в уравнении связи, а само уравнение хорошо отражает структуру СК-ПСА.
Нами получено еще одно, 2-е уравнение связи для остальных двух квантовых чисел (из полного набора в соответствии с принципом запрета В.Паули) - m l и m s , но о них в двух словах не скажешь, да и с физическим смыслом "спинового" квантового числа m s нужно ещё разобраться - об этом см.
Начало (порядковый номер исходного элемента - Z M ) каждой M-диады (пары периодов СК-ПСА) можно получить из выполненного автором тождественного преобразования формулы В.М. Клечковского для номера Z l элемента, при котором впервые появляется элемент с данным значением l max
Z M = Z l -1 = = ,
тогда при l max = 0; 1; 2; 3; 4... имеем Z M = 0; 4; 20; 56; 120..., т.е. это так называемые тетраэдрические числа, что опосредованно связано с некими минимальными исходными для диады квантовыми энергетическими уровнями (тетраэдр среди всех пространственных тел имеет минимальную площадь поверхности при фиксированном объёме).
Более подробно на эту тему и упомянутых двух уравнениях связи квантовых чисел автор предполагает сообщить в готовящихся к печати работах .
Автор не претендует этой работой, естественно, на создание полной теории Периодической системы нейтральных атомов и ее математического выражения, но считает ее необходимым и важным этапом на этом пути, и в меру своих сил будет содействовать дальнейшему продвижению.
СПИСОК ЛИТЕРАТУРЫ:
- Клечковский В.М. «Распределение атомных электронов и правило последовательного заполнения (n + l )- групп», М., Атомиздат, 1968
- Клечковский В.М. «Развитие некоторых теоретических проблем Периодической системы Д.И. Менделеева" (доклад на симпозиуме Х Менделеевского съезда). М., Наука, 1971, стр. 54-67.
- Трифонов Д.Н. "Структура и границы периодической системы", М., Атомиздат, 1976, 271 стр.
- Махов Б.Ф., книга "Симметричная квантовая Периодическая система элементов" (СК-ПСЭ), Москва, 1997 - ISBN 5-86700-027-3
- Махов Б.Ф., Статья «Симметричная квантовая периодическая система элементов (нейтральных атомов) - СК-ПСА (или Новая периодизация Периодической системы», в журнале РАЕ «Фундаментальные исследования», 2007, № 9, с. 30-36 - ISSN 1812-7339
- Махов Б.Ф., Доклад «Проявление парности в Периодической системе нейтральных атомов (СК-ПСА)», в Трудах V-Межд. конференции «Биниология, симметрология и синергетика в естественных науках», сент. 2007, г. Тюмень, ТюмГНГУ, Раздел «Физика и химия», стр. 59-65 ISBN 978-5-88465-835-4
- Махов Б.Ф., Статья «Мировой эфир» Д.И. Менделеева и его место в Периодической системе», в журнале РАЕ «Фундаментальные исследования», 2008, № 3, с. 25-28
- Махов Б.Ф., Статья «Физическая природа металлов в свете колебательной модели атома», в журнале РАЕ «Фундаментальные исследования», 2008, № 3, с. 29-37
- Ландау Л.Д., Лифшиц Е.М. «Квантовая механика. Нерелятивистская теория», М.: Наука, 1974 (3-е изд). стр. 293. и 1989 (4-е изд). стр. 302
- Махов Б.Ф., книга "О модели нейтрального атома и путях выхода из кризиса в атомной физике» (подготовлена к печати).
- Махов Б.Ф., книга «Трехмерная СК-ПСА» (подготовлена к печати).
- Бронштейн И.Н., Семендяев К.А., Справочник по математике для инженеров и учащихся втузов. М.: Наука, Гл.ред. ФМЛ, 1986 (13е,испр), стр.127
- Статья "Тонкой структуры постоянная", Физический энциклопедический словарь - ФЭС, с.763
Библиографическая ссылка
Махов Б.Ф. ПЕРИОДИЧЕСКИЙ ЗАКОН Д.И. МЕНДЕЛЕЕВА – НОВАЯ ФОРМУЛИРОВКА И МАТЕМАТИЧЕСКОЕ ВЫРАЖЕНИЕ ЗАКОНА // Успехи современного естествознания. – 2008. – № 9. – С. 24-29;URL: http://natural-sciences.ru/ru/article/view?id=10547 (дата обращения: 29.02.2020). Предлагаем вашему вниманию журналы, издающиеся в издательстве «Академия Естествознания»